Reaktionsmechanismen
Es gibt im Prinzip drei verschiedene Reaktionsmechanismen: Addition, Substitution und Eliminierung. Diese Reaktionsmechanismen können elektrophil, nukleophil oder radikalisch verlaufen. Im Folgenden werden die elektrophile Addition, die radikalische Substitution und eine Eliminierungsreaktion im Detail erklärt.
Elektrophile Addition
Die Elektrophile Addition verläuft in zwei Schritten.
1. Elektrophiler Angriff
Ein Molekül wird durch eine hohe Elektronendichte (z.B. einer Mehrfachbindung) eines anderen Moleküls polarisiert und angezogen. Dieses wird in einem Übergangszustand an das angegriffene Molekül gebunden. Aus diesem Zustand trennt sich ein Anion, während das Kation des angreifenden Moleküls am gebunden bleibt und durch Mesomerie stabilisiert wird.
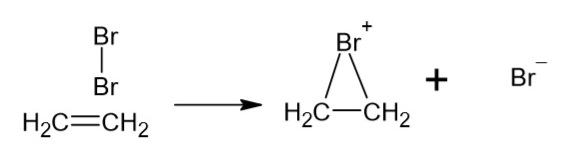
2. nukleophiler Rückseitenangriff
Das verbliebene Anion wird vom Molekül angezogen und lagert sich auf der Rückseite des Gesamtkations an.

Wird Wasser einem Molekül zugefügt, so nennt man dies "Hydratisierung". Ist das zugefügte Molekül Wasserstoff, so wird dies "Hydrierung" genannt.
Radikalische Substitution
Die radikalische Substitution besteht aus Startreaktion, Kettenreaktion und Abbruchreaktion.
1. Startreaktion
In der Startreaktion wird ein Halogenmolekül homolytisch in zwei Moleküle gespalten. Dies bedeutet, dass die Elektronen der gespaltenen Elektronenpaarbindung sich gleichmäßig auf beide entstandenen Molekäle aufteilen. Somit entstehen zwei Molekäle mit einem ungepaarten Elektron, auch "freie Radikale" genannt.
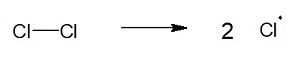
2. Kettenreaktion
Während der Kettenreaktion greift eines dieser freien Radikale ein Alkan an und geht eine Bindung mit einem Wasserstoffatom ein. Das verbleibende Alkan hat nun ein ungepaartes Elektron und ist zum Radikal geworden. Dieses Radikal kann nun ein weiteres Halogen oder Alkan aufsuchen und angreifen, sodass immer wieder neue Radikale entstehen. So kann diese Kettenreaktion immer weiterlaufen.
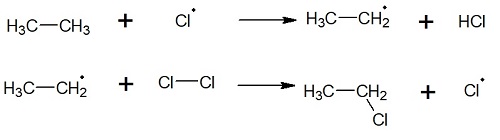
3. Abbruchreaktion
Es kommt zur Abbruchreaktion, wenn zwei Radikale miteinander reagieren. Dabei entstehen keine neuen Radikale.
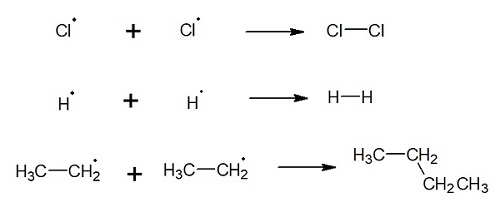
Eliminierung
In einer Eliminierungsreaktion werden aus einem Molekül zwei Atome oder Atomgruppen abgespalten. Oft werden zwei benachbarte Atome abgespalten, sodass eine Mehrfachbindung entsteht. Die Eliminierung erfolgt für gewöhnlich in drei Schritten. Zunächst wird ein Molekül protoniert, daraufhin bildet sich ein Carbenium-Ion und schließlich wird das Molekül deprotoniert.
1. Protonierung:
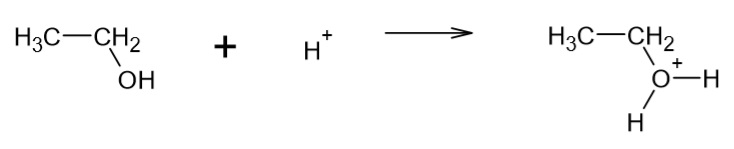
2. Bildung Carbeniumion:
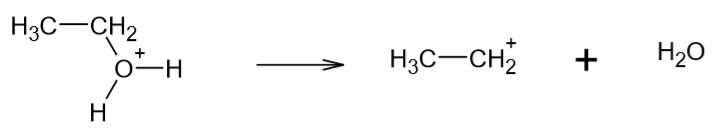
3. Deprotonierung:
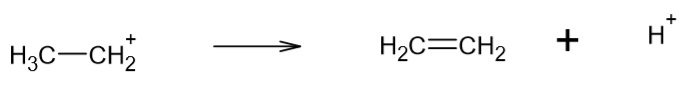
Wenn zwei Wasserstoffatome abgespalten werden, nennt man dies "Dehydrierung". Wird Wasser als Molekül abgespalten, wird dies "Dehydratisierung" genannt.
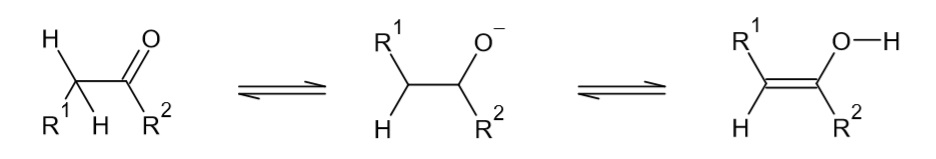
Tautomerie
Die Tautomerie ist eine Umlagerungsreaktion. Dabei werden die Atome eines Moleküls neu gruppiert, sodass eine neue chemische Verbindung entsteht. In einigen Fällen wird eine Bindung zwischen zwei Kohlenstoffatomen gepalten und danach eine neue C-C-Bindung an einer anderen Stelle ausgebildet. Wenn aus einem Keton ein Alkanol oder anderes herum entsteht, wird dies "Keto-Enol-Tautomerie" genannt.